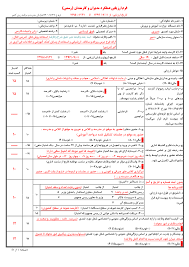
تحقیق در مورد فنول
فنول
|
شناساگرها |
|
|
SJ3325000 |
|
|
جیمول-تصاویر سه بعدی |
|
|
خصوصیات |
|
|
C6H6O |
|
|
۹۴٫۱۱ g mol−1 |
|
|
شکل ظاهری |
جامد کریستالی سفید رنگ |
|
1.07g/cm³ |
|
|
۴۰٫۵درجه سلسیوس (۱۰۴٫۹ درجه فارنهایت; ۳۱۳٫۶ کلوین |
|
|
181.7 °C, 455 K, 359 °F |
|
|
اسیدی (pKa) |
9.95 |
|
1.7 D |
|
|
خطرات |
|
|
سمی (T) |
|
|
|
|
|
79°C |
|
|
ترکیبات مرتبط |
|
|
ترکیبات مرتبط |
|
|
به استثنایجایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیتاستانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) |
|
فنول یکی از ترکیبات ساده آلی بوده که از اتصال یک گروه هیدروکسیل و یک حلقه بنزنی تشکیل می شود.فنول با فرمول(C۶H۵OH) با نامهای هیدروکسی بنزن(hydroxyl benzene) وکربولیک اسید (carbolic acid) نیز شناخته می شود.فنول خالص جامدی سفید رنگ با دمای ذوب۴۲°C یا ۱۰۸°F است.فنول به طور معمول قابل انحلال در آب میباشد و خاصیت اسیدی ضعیفی دارد (pKa=9.9).فنول به عنوان یک گند زدا استفاده می شود.فنول با غلظت بالا میتواند باعث سوختگی پوست شود.ترکیباتی که در آن بیش از یک گروه هیدروکسیل متصل به حلقه بنزن باشد را ترکیبات پلی هیدریک فنول(poly hydric phenols)می نامند.فنول یکی از ترکیبات مهم آلی مورد استفاده در صنعت است.فنول در بسیاری از صنایع به عنوان ماده اولیه کاربرد دارد.برخی از موادی که از این ماده تولید می شوند عبارتند از: نایلون، شوینده ها، افرودنیهای بنزین، آسپرین، پلی اورتان، رنگها، علف کشها، نرم کننده ها، ضد اکسنده ها، روغنهای روان کننده، قارچ کش ها.[۱]
خواص فیزیکی
فنولها مایع یاجامدهایی با دمای ذوب پایین هستند.دمای جوش آنها به علت پیوند هیدروژنی، کاملاً بالاست.خود فنول(C۶H۵OH)احتمالاً به علت تشکیل پیوند هیدروژنیبا آب، کمی درآن انحلال پذیر است (9 گرم در 100 گرم آب) .بیشتر فنولهای دیگر اساساً در آب انحلال ناپذیرند.فنولها بی رنگ هستند مگر آنکه گروهی مولد رنگ وجود داشته باشد.[۲]
اثرات فنول بر بدن انسان
در صورت تنفس یا خورده شدن این ماده توسط انسان این ماده وارد گردش خون خواهد شد و در صورت تماس با پوست کمتر وارد خون خواهد شد.قرار گرفتن در معرض فنول در کوتاه مدت می تواند باعث سوزش چشمها و سر درد شود.افرادی که تماس پوستی با مقدار زیادی از فنول دارند، سوزش پوست، ضایعات کبدی، ادرار تیره و ضربان نا منظم قلب در آنها مشاهده می شود. بلعیدن مقدار زیادی از فنول می تواند باعث سوختگیهای داخلی و مرگ شود. اما فنول می تواند در علم پزشکیبه عنوان یک ماده بی هوش کننده و همچنین یک ماده ضد عفونی کننده مورد استفاده قرار گیرد. همچنین آژانس بینالمللی تحقیقات سرطان(به انگلیسی: International Agency for Research on Cancer) فنول را به عنوان ماده ای غیر سرطان زا طبقه بندیکرده است.[۳]
منابع
1.
Concise Encyclopedia of Chemistry (2004) . McGraw-Hill.ISBN 0-07-143953-6
موریسون، رابرت تورنتون، رابرت نیلسون بوید.شیمی آلی ۲.تهران:نشر علوم دانشگاهی
|
خواص فیزیکی الکلها |
|
|
|
گروه -OH در یک نوع الکل |
دید کلی
فرمول عمومی الکلها، ROHاست که در آن ، Rیک گروه آلکیل یا آلکیل استخلاف شده است. این گروه میتواند نوع اول ، دوم یا سوم باشد. ممکن است زنجیر باز یا حلقهای باشد؛ ممکن است دارای یک اتم هالوژن، هیدروکسیلهای بیشتر یا یکی از بسیاری گروههای دیگر باشد که در شیمی آلیوجود دارد
همه الکلها ، دارای گروه هیدروکسیل ( -OH ) هستند که بهعنوان گروه عاملی ، خواص مشخصه این خانواده از ترکیبها را تعیین میکند. تغییر و تنوع در ساختار Rمیتواند بر سرعت واکنشهای الکلها و حتی در موارد معدودی ، بر نوع واکنشها تاثیر گذارد. باید توجه داشت که ترکیباتی که در آنها گروه هیدروکسیل مستقیما به یک حلقه آروماتیک متصل است، الکل نیستند؛ آنها فنل هستند و با الکلها تفاوت فاحشی دارند.
گروه عاملی -OH
اگر این واقعیت را در نظر داشته باشیم که از نظر ساختاری: الکل آمیزه ای از یک آلکانو آباست، بهخوبی میتوانیم خواص فیزیکی الکلها را درک کنیم. الکل متشکل از یک گروه آلکیل شبه آلکان و یک گروه هیدروکسیل شبه آب است. از دو واحد ساختاری الکل ، این گروه -OH است که سبب خواص فیزیکی مشخصه آب میشود و گروه آلکیل ، بسته به اندازه و شکلش ، این خواص را تعدیل میکند.
گروه هیدروکسیل کاملا قطبی است و نکته بسیار مهم اینکه ، دارای هیدروژنی است که به عنصر بهشدت الکترونگاتیو اکسیژنپیوند دارد. یک الکل با استفاده از گروه هیدروکسیل میتواند پیوند هیدروژنی تشکیل دهد، پیوند هیدروژنی با مولکولهای الکل همانندش و با مولکولهای خنثی و با آنیونها.
دمای جوش
در میان هیدروکربنهابه نظر میرسد که عوامل تعیین کننده دمای جوش ، عمدتا وزن مولکولی و شکل مولکولی باشند؛ این چیزی است که از مولکولهایی که عمدتا با نیروهای واندروالسی در کنار یکدیگرند، انتظار میرود. در الکلها نیز با افزایش تعداد کربن ، دمای جوش بالا میرود و با شاخهدار شدن زنجیر ، دمای جوش پایین میآید. اما نکته غیر عادی ، در مورد الکلها این است که آنها در دمایی بالا به جوش میآیند.
این دماهای جوش ، بسیار بالاتر از دمای جوش هیدروکربنها با وزن مولکولی یکسان است و حتی از دمای جوش بسیاری ترکیبها با قطبیت قابل ملاحظه بالاتر است. چگونه این پدیده را تبیین میکنیم؟ بدیهی است پاسخ این است که الکلها ، همانند آب ، مایعهای بهم پیوسته هستند. دمای جوش بالای آنها به علت نیاز به انرژی بیشتر برای شکستن پیوندهای هیدروژنی است که مولکولها را در کنار یکدیگر نگه داشتهاند. اگر چه اترها و آلدئیدها هم اکسیژن دارند، اما هیدروژن در آنها فقط با کربن پیوند دارد ، این نوع هیدروکربنها آنقدر مثبت نیستند که بتوانند با اکسیژن ، پیوند قابل ملاحظه ای ایجاد کنند.
|
|
|
ساختمان اتانول |
مطالعه پیوند هیدروژنی در الکلها
در مطالعه پیوند هیدروژنی ، طیف بینی زیر قرمز ، نقش کلیدی بر عهده داشته است. در محلول رقیق در یک حلال غیر قطبی مانند کربن تتراکلرید (یا در فاز گاز) ، یعنی در حالتی که تجمع مولکولی ، کمینه است، به عنوان مثال ، اتانول ، نوار کششی O-H را در 3640cm-1 نشان میدهد. با افزایش غلظت اتانول ، بتدریج ، نوار پهنتر دیگری در 3350cm-1 جایگزین این نوار میشود. پیوند هیدروژنیبا اکسیژن دوم ، پیوند O-H را تضعیف میکند و انرژی و بتبع آن ، فرکانس ارتعاش را پایین میآورد.
حل شدن الکلها
رفتار الکلها بهعنوان حل شده نیز ، توانایی آنها برای تشکیل پیوند هیدروژنی را منعکس میکند. برخلاف هیدروکربنها ، الکلهای سبک با آب امتزاجپذیرند. از آنجا که نیروهای بین مولکولی الکلها ، همانند نیروهای بین مولکولی آب است، دو نوع مولکول با یکدیگر قابل اختلاطند: انرژی لازم برای شکسیتن یک پیوند هیدروژنی بین دو مولکول آب یا دو مولکول الکل ، با تشکیل یک پیوند هیدروژنی بین یک مولکول آب و یک مولکول الکل تامین میشود. اما این موضوع ، فقط در مورد اللکهای سبک ، یعنی الکلهایی که در آنها گروه -OH بخش بزرگی از مولکولرا تشکیل میدهد، صادق است.

با بزرگتر شدن گروه آلکیل شبه آلکان ، انحلال پذیریدر آب کاهش مییابد. از دیدگاه عملی ، خط مرزی بین انحلال پذیری و انحلال ناپذیری الکلهای نوع اول در آب را الکل چهار تا پنج کربنی در نظر میگیریم. الکلهای پلیهیدروکسی در هر مولکول بیش از یک موضع برای تشکیل پیوند هیدروژنی دارند و این ویژگی در خواص آنها منعکس است. ساده ترین دیول ، 1، 2 اتاندیول ، (اتیلن گلیکول) در 197درجه سانتیگراد میجوشد.
دیولهای سبک با آب در میآمیزند و آنهایی که تا هفت اتم کربن دارند، در آب انحلالپذیری قابل ملاحظه ای دارند. خاصیات ضد انجماد اتیلن گلیکول ناشی از دمای جوش بالا ، دمای انجماد پایین و انحلالپذیری بالا در آب است.
منبع
- شیمی آلی ، جلد اول ؛ تالیف: موریسون ، بوید. نشر علوم دانشگاهی.
|
هیدروکربنهای آروماتیک چند هستهای |

|
بطور کلی هیدرو کربنهاییکه خواص بنزنمانند از خودشان نشان میدهند، هیدروکربنهای آروماتیک نامیده میشوند و آنهایی که حلقههای جوش خورده بنزندارند، هیدروکربنهای آروماتیک چندحلقهای یا پلیسیکلیک نامیده میشوند. بسیاری از PAH ها مانند بنزن پایداری بالا و ساختار هندسی مسطح دارند. از میان هیدروکربنها فقط نفتالین بصورت تجاری تولید میشود. برخی از PAH ها در مشتقات قطران زغالسنگ یافت میشوند. |
ساختار PAH ها
PAH ها از دو یا چند حلقه شش عضوی تشکیل شدهاند که این حلقهها بوسیله اشتراک یک جفت اتمهای کربنمجاور بین حلقهها جوش خورده و بهم متصل شدهاند. سادهترین عضو این گروه ، نفتالین C10H8است. به کربنهای مشترک بین دو حلقه ، اتم هیدروژن متصل نیست. نفتالین ، جامد فراری است که بخار آن برای برخی حشرات، سمی است و بهعنوان ضد بید بکار میرود.
آنتراسن(دارای سه حلقه بنزن بصورت خطی) و فنانترن (دارای سه حلقه ولی بصورت انشعابی) ، هر دو جزو آلایندههای مربوط به احتراقناقص چوبو زغال سنگهستند و از پالایشگاههای نفت و کورههای زغالسنگ به محیط زیست وارد میشوند.
مکانیسم تشکیل PAH در جریان احتراق
مکانیسم تشکیل PAH در جریان احتراق پیچیده است، اما ظاهرا بطور عمده به علت بسپارش (پلیمریزاسیون) مجدد قطعههای هیدروکربنیاست که به هنگام کراکینگ یعنی شکسته شدن مولکولهای بزرگتر سوخت در اثر گرما به چندین قسمت تبدیل میشوند. این قطعات هیدروکربنی با کاهش نسبت اکسیژنبه سوخت ، دوباره با یکدیگر ترکیب میشوند و با از دست دادن هیدروژن، قطعههای غنی از کربن به یکدیگر جوش خورده ، ترکیبات هیدروکربنی آروماتیک چند هستهای را تشکیل میدهند که مولکولهای بسیار پایداری بشمار میروند.
PAH ها به عنوان آلایندههای هوا
این ترکیبات از آلایندههای متداول هوا هستند و در شهرهای بزرگ و صنعتی ، غلظت آنها در هوا روز به روز بیشتر میشود. PAH هایی که تعداد حلقههایشان 4 یا کمتر از آن است وقتی رها میشوند در هوا بصورت گاز باقی مانده و معمولا کمتر از یک روز توسط واکنشهای رادیکالی تخریب میشوند. اما PAH های با بیش از 4 حلقه بنزن بر خلاف همردههای کوچکتر خود برای مدت طولانی در هوا به صورت مولکولهای گازی دوام نمیآورند و بعلت کم بودن فشار بخاربه سرعت متراکم شده ، جذب سطحی دوده و خاکستر میشوند و بعلت ریز بودن برخی ذرات دوده ، ممکن است از راه تنفس وارد ششها شوند.
PAH ها به عنوان آلایندههای آب
هیدروکربنهای آروماتیک پلیسیکلیک همچنین از آلایندههای جدی آببشمار میروند. PAH ها به مقدار قابل ملاحظهای در تولید مشتقات قطران زغالسنگ مانند کرئوزوت که محافظ چوب است، بوجود میآید. استفاده از کرئوزوت برای محافظت الوارهای غوطهور در آب لنگرها باعث نفوذ PAH ها به آب و باعث آلودگی سختپوستان میشود. این ترکیبات همچنین از ریخته شدن نفتاز نفتکشها و پالایشگاهها و محلهای حفر چاه واقع در فلات قاره ، وارد محیط زیست آبیمیشوند. PAH های بزرگتر در بافتهای چربی برخی موجودات دریایی تجمع زیستی دارند.

منبع مهم PAH
گازهای خروجی از موتورهای بنزین سوز و دیزلی ، قطران دود سیگار ، سطح غذای سوخته ، دود ناشی از سوختن چوب یا زغال سنگ یا سایر فراوردههای احتراق که در آنها کربن موجود در سوخت بطور کامل به COیا CO2تبدیل نمیشود، از منابع PAHها هستند. اگر چه این مواد تنها حدود 0.1 % مواد معلق موجود در هوا را تشکیل میدهند، وجود آنها بهعنوان آلایندههای جویموجب نگرانی است.، زیرا شواهدی از سرطانزایی آنها دستکم در حیوانات آزمایشگاهی در دست است.
دوده
دوده بطور عمده ، کربن گرافیت مانند است و از خرده بلورهایی که هر کدام از آنها از لایههای روی هم انباشته اتمهای کربن است، تشکیل یافته است که تمام آنها در حلقههای جوش خورده بنزن شرکت دارند. گرافیت ، PAH نهایی است. هر کدام از صفحههای موازی حلقههای جوش خورده بنزن دارای تعداد بیشماری اتمهای کربن است. در گرافیت هیچ اتم هیدروژنی بجز در پیرامون لایهها وجود ندارد. سطوح ذرههای دوده ، جاذبههای مناسبی برای مولکولهای گازی است.
منبع : سايت علمی و پژوهشي آسمان -- صفحه اینستاگرام ما را دنبال کنیداين مطلب در تاريخ: یکشنبه 14 تیر 1394 ساعت: 8:56 منتشر شده است
برچسب ها : تحقیق در مورد فنول,
 را بنویسید.
را بنویسید.






.png)
_285282.jpg)